発表のポイント
- 光に反応してカリウムイオンを選択的に輸送するタンパク質(カリウムチャネルロドプシン:Kalium channelrhodopsin, KCR)の立体構造を、クライオ電子顕微鏡を用いて解明しました。
- KCRはイオン透過経路の細胞外側に存在するイオン選択フィルター、細胞内側に存在する脱水和システム、そして生理的条件下において形成されるイオン濃度勾配という3要素を利用することで高いカリウムイオン選択性を実現させているという、既知のカリウムイオンチャネルとは全く異なるKCR独自のイオン選択機構を明らかにしました。
- 立体構造情報に基づき創出した、カリウムイオン選択性をさらに向上させたKCR変異体(KALI)は、次世代の光遺伝学実験を可能にするツールとして神経科学や遺伝子治療の発展に貢献することが期待されます。
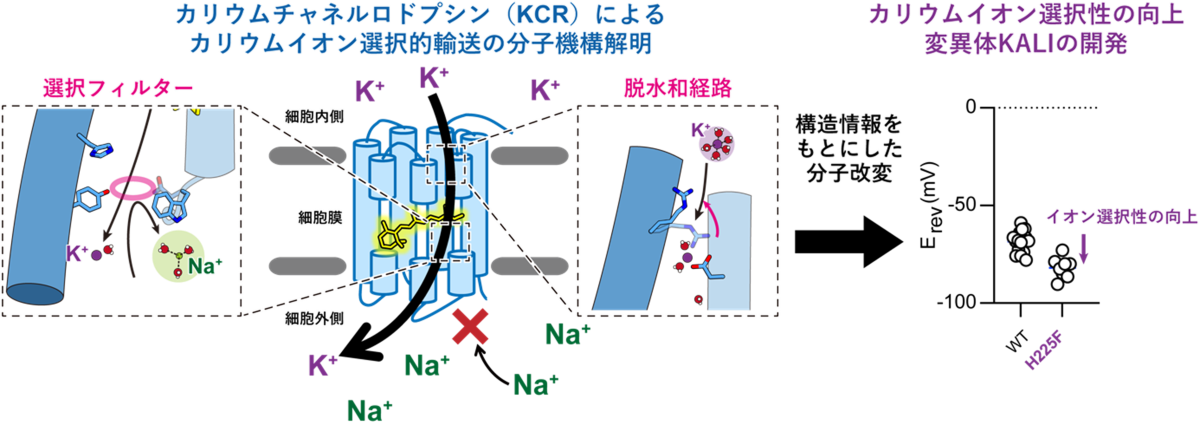
本研究の概略
発表概要
光刺激によってイオンを輸送する膜タンパク質であるチャネルロドプシン(注1、2)は、実験動物の神経活動を生きたまま光制御する「光遺伝学ツール(注3)」として広く利用されてきました。近年カリウムイオンを選択的に輸送するカリウムチャネルロドプシン(KCR、注4)が発見され、神経活動を抑制する理想的な光遺伝学ツールとして期待されています。しかし、KCRは既知のカリウムイオンチャネルとはあらゆる面で全く異なっており、KCRがどのようにカリウムイオンを選択的に輸送するかは大きな謎となっていました。
東京大学大学院総合文化研究科の但馬聖也大学院生、岸孝一郎大学院生、福田昌弘特任助教、加藤英明准教授、同大学物性研究所の井上圭一准教授、名古屋工業大学大学院工学研究科の杉浦雅大大学院生、片山耕大准教授、神取秀樹特別教授らの研究グループは、クライオ電子顕微鏡(注5)を用いてKCRの立体構造決定に成功しました。電気生理学(注6)、分光学(注7)及び計算科学(注8)を組み合わせることで、KCRは細胞外側の選択フィルター(注9)、細胞内側の脱水和システム、そして生理的条件下で形成されるイオン濃度勾配を利用することにより、高いカリウムイオン選択性を実現していることが明らかとなりました。
既知のカリウムイオンチャネルによるイオン選択性のしくみは1998年にRoderick MacKinnon博士らによって解明され、同氏は2003年にノーベル化学賞を受賞しましたが、本研究成果ではおよそ四半世紀ぶりに、生物が有する全く新たなカリウムイオン選択機構を解明したことになります。さらに、本研究グループが開発したカリウムイオン選択性をさらに向上させたKCR変異体(KALI)は、次世代の光遺伝学実験を可能にするツールとして神経科学や遺伝子治療の発展に貢献することが期待されます。
本研究成果は、2023年8月30日(米国東部夏時間)に米国科学誌「Cell」のオンライン版に掲載されました。
発表詳細
大学院総合文化研究科のページからご覧ください。
発表者
東京大学
大学院総合文化研究科
加藤 英明(准教授)〈兼:大学院理学系研究科〉
福田 昌弘(特任助教)
但馬 聖也(博士課程)
岸 孝一郎(博士課程)
物性研究所
井上 圭一(准教授)
名古屋工業大学
大学院工学研究科
神取 秀樹(特別教授)
片山 耕大(准教授)
杉浦 雅大(博士課程)
Stanford大学
Department of Bioengineering
Karl Deisseroth(Professor)
Yoon Seok Kim(Postdoctoral researcher)
YoungJu Jo(Graduate student in PhD program)
Peter Wang(Postdoctoral researcher)
Department of Computer Science
Ron Dror(Professor)
Joseph Paggi(Graduate student in PhD program)
用語説明
(注1)ロドプシン
ヒトから微生物まで多くの生き物が持つ光受容タンパク質。共通構造として7本の膜貫通へリックスを有する膜タンパク質であり、中心に光吸収を担う発色団としてレチナールと呼ばれる小分子を結合している。
(注2)チャネルロドプシン
ロドプシンの中でも、光刺激に応じてイオンの電気化学勾配に従ってイオンを輸送する「イオンチャネル」として機能するもの。2002年に藻類から発見された。細胞膜は脂質二重膜で構成されているため本来イオンをほとんど透過できないが、細胞膜中に存在するイオンチャネルと呼ばれる膜タンパク質によって細胞内外の濃度勾配に応じたイオンの輸送が可能となる。
(注3)光遺伝学(オプトジェネティクス)
opto(光)とgenetics(遺伝学)を組み合わせた言葉であり、遺伝学の手法を用いて特定の神経細胞に光受容タンパク質を発現させ、光によって神経細胞の活動を制御する技術。Stanford大学のKarl Deisseroth博士らによって実現された。
(注4)KCR(Kalium channelrhodopsin)
生理的に重要なイオンのひとつであるカリウムイオンを選択的に輸送するチャネルロドプシン。2022年に初めて自然界より発見された (Govorunova et al., Nat. Neurosci. (2022))。報告されたHcKCR1とHcKCR2は、ナトリウムイオンと比較しカリウムイオンに対して約20倍高い透過性を示し、神経を抑制する光遺伝学ツールとしての利用が期待されている。
(注5)クライオ電子顕微鏡
2017年にノーベル化学賞を受賞した技術。一般的な光学顕微鏡とは異なり、極低温環境(クライオ)でタンパク質サンプルに電子線を照射し、その投影像から立体構造を計算して求める手法。この手法によって、タンパク質の構造解析にかかる時間が大幅に短縮され注目を集めている。
(注6)電気生理学
イオンチャネルの性質を調べるための実験技術。透過するイオンの種類(イオン選択性)の他に、チャネルが開いたり閉じたりするまでの時間(キネティクス)、光や電位に対する応答性を詳細に調べることができる。
(注7)分光学
サンプルに光を照射し、その透過光や散乱光を解析することで1原子レベルで分子の状態を調べることができる実験技術。ロドプシンは光を吸収する性質があるため分光学との相性がよく、古くから分光学を用いてロドプシンの分子解析が行われてきた。
(注8)計算科学
実験では調べることが難しいタンパク質の動き(ダイナミクス)や、励起などの量子化学的な現象を計算によってシミュレーションする手法。
(注9)選択フィルター
イオンチャネルに見られる特定のイオンを選択的に透過するための構造。カリウムイオンチャネルの構造は1998年にRockefeller大学のRoderick MacKinnon博士らにより初めて報告され、以降様々なカリウムイオンチャネルの構造が報告されてきた。これまで知られているカリウムイオンチャネルはすべて共通して多量体を形成し、その界面に対称的な構造を有する選択フィルターを有する。この選択フィルターにおいて、カリウムイオンはエネルギー的に最安定な配位構造をとることができる一方で、よりイオン半径が小さいナトリウムイオンはその配位構造が選択フィルター内で不安定化されるため効率的に選択フィルターを透過できない。このようなカリウムイオンチャネルが選択的にカリウムイオンを輸送するしくみの解明をはじめとしたイオンチャネル研究の功績が認められ、同博士を含む2名の研究者が2003年にノーベル化学賞を受賞している。
論文情報
Seiya Tajima, Yoon Seok Kim, Masahiro Fukuda, YoungJu Jo, Peter Y. Wang, Joseph M. Paggi, Masatoshi Inoue, Eamon F.X. Byrne, Koichiro E. Kishi, Seiwa Nakamura, Charu Ramakrishnan, Shunki Takaramoto, Takashi Nagata, Masae Konno, Masahiro Sugiura, Kota Katayama, Toshiki E. Matsui, Keitaro Yamashita, Suhyang Kim, Hisako Ikeda, Jaeah Kim, Hideki Kandori, Ron O. Dror, Keiichi Inoue, Karl Deisseroth*, Hideaki E. Kato*, "Structural basis for ion selectivity in potassium-selective channelrhodopsins," Cell: 2023年8月30日, doi:10.1016/j.cell.2023.08.009.
論文へのリンク (掲載誌)
関連リンク
原文URL:https://www.u-tokyo.ac.jp/focus/ja/press/z0109_00092.html
